光合成
光合成(こうごうせい、独: Photosynthese、仏: photosynthèse、拉、英: photosynthesis)は、主に植物や植物プランクトン、藻類など光合成色素をもつ生物が行う、光エネルギーを化学エネルギーに変換する生化学反応のことである[1]。光合成生物は光エネルギーを使って水と空気中の二酸化炭素から炭水化物(糖類:例えばショ糖やデンプン)を合成している。また、光合成は水を分解する過程で生じた酸素を大気中に供給している。年間に地球上で固定される二酸化炭素は約1014kg、貯蔵されるエネルギーは1018kJと見積もられている[2]。
「光合成」という名称を初めて使ったのはアメリカの植物学者チャールズ・バーネス(1893年)である[3]。
ひかりごうせいとも呼ばれることが多い。かつては炭酸同化作用(たんさんどうかさよう)とも言ったが[4]現在はあまり使われない。
Contents
光合成の発見
1648年にフランドルの医師であるヤン・ファン・ヘルモントは、鉢植えのヤナギに水だけを与えて成長させる実験を行った[5]。生育前と後では鉢植えの土の重量がほとんど変わらなかったため彼は「木の重量増加は水に由来する」と考えた。質量保存の法則が確立する1世紀も前のことであった。
1771年、イギリスの化学者および聖職者であるジョセフ・プリーストリーは、「植物はきれいな空気を出して空気を浄化している」と考えた。彼は、密閉したガラス瓶の中でロウソクを燃やして「汚れた空気」をつくり、そこにハッカとネズミを入れたものとネズミだけを入れたものを用意した。するとハッカを入れた方のネズミは生き続けたが、入れない方のネズミは数秒で気絶、その後死亡した。この実験結果を元に彼は「呼吸で汚れた空気を浄化する何かがある」と考えたのである。彼はその後1774年に酸素を発見し[3]、「脱フロギストン空気」と名付けた[2]。しかし、酸素の燃焼と呼吸での役割を解明したのはアントワーヌ・ラヴォアジエである。さらに、ラヴォアジエは酸素(oxygen)と二酸化炭素(carbon dioxide)の名付け親でもある。
1779年、ジョセフ・プリーストリーの発見に影響を受けたオランダの医師ヤン・インゲンホウスは、水草による実験を行った。当時、水草から発生する気体は「ふつうの空気」であると考えられていた。しかし、彼はこの気体を集めて火を入れてみたところ勢いよく燃える事を発見した。次に、日光の当たる場所と暗闇に置いた場合の水草を比べてみたところ、前者からは気体が発生したが、後者からは気体は発生しなかった。このような実験の結果から、彼は「植物の空気浄化能は葉の緑色部分であり、光の影響を受ける」ことを発見した。また彼は、火を燃やすことができる「きれいな空気」と植物を入れた容器を暗闇に置くと、その容器内の空気が燃焼が起きない「汚れた空気」に変わることも発見している。今で言う「呼吸」が起こっていたのである。
1782年、スイスの司祭ジャン・セネビエは、当時「固定空気」(common air)と呼ばれていた二酸化炭素が光合成で取り込まれることを示し[2]、二酸化炭素は根から取り込むと考えた[3]。
1804年、同じくスイスのニコラス・テオドール・ド・ソシュールは、ジャン・セネビエの二酸化炭素は土から取り込まれるという考えに疑問を持ち、ソラマメを土ではなく小石の上で育てる実験を行った。するとソラマメは普通に育ったため、植物は空気から二酸化炭素を得ていることが分かった。また、植物の枝(使われたのはLonicera caprifolium、Prunus demestica、Ligustrum vulgare、Amygdalus persica の4種)を二酸化炭素を吸収する石灰と同封して育てたところ葉がすべて落ちてしまったことから、植物は二酸化炭素が無いと生きていけないことを発見した。さらに、有機物と酸素の総重量が植物が取り込んだ二酸化炭素の重量よりも大きいことも発見、光合成には水が必要であるとし、以下の式を導いた。(当時はまだ化学式が使われていなかったため言葉の式となっている)
- 二酸化炭素 + 水 → 植物の成長 + 酸素
1842年には、ドイツの物理学者ユリウス・ロベルト・フォン・マイヤーによって、光合成は「光エネルギーを化学エネルギーに変換している」ことがつきとめられた。
1862年、ドイツの植物生理学者ユリウス・フォン・ザックスは、葉緑体を顕微鏡で見たときに現れる白い粒は取り込まれた二酸化炭素に関係があるのではないかと考えた。彼は当時既に知られていたヨウ素デンプン反応を参考に、日光に十分当てた葉にヨウ素液をつけた。すると葉は紫色に変色した。この結果から彼は「植物は日光が当たると二酸化炭素を取り込んで葉緑体の中でデンプンを作り、それを使って生きている」ことを発見したのである。
葉緑体(クロロプラスト)
1, 外膜
2, 膜間部
3, 内膜
4, ストロマ
5, チラコイドルーメン
6, チラコイド膜
7, グラナ
8, チラコイドラメラ
9, デンプン
10, リボソーム
11, DNA
12, プラスト顆粒(脂質の玉)
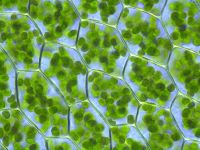
光合成を行っているのは葉緑体の中の細胞小器官である。葉緑体は細胞内に1〜1000個ほど存在し、大きさも形もさまざまである。最も平均的なのは長さ約5μmの回転楕円体状のものである。葉緑体は全透性の外膜と半透性の内膜の二重膜で囲まれている。内膜の内部のことをストロマという。ストロマには酵素、DNA、RNA、リボソーム、そして膜で囲まれたチラコイドがある。チラコイド膜の内部はチラコイドルーメンという。チラコイドは積み重なってグラナを構成し、グラナ同士はところどころでチラコイドラメラ(またはストロマチラコイド)で繋がっている。グラナの数は10〜100程度である。チラコイド膜は葉緑体の内膜が陥入することで作られる[2]。
チラコイド膜の組成は特殊で、リン脂質は10%しかない。膜の構成成分で一番多く、全体の80%を占めているのは糖脂質(ガラクトシルジアシルグリセロールとジガラクトシルジアシルグリセロール)である。そして残りの10%はスルホリピド(6-スルホキノボシルジアシルグリセロール)とキノボース(6-デオキシグルコース)である。チラコイド膜の脂質は高度に不飽和であるため流動性が大きい[2]。葉緑体は光の強弱に反応して細胞内を移動することができ、強光下では光阻害を避け、弱光下では光を捕集するように配置を変える。このとき光受容体となるのが、青色光受容体(フォトトロピン)である。葉緑体の運動にはアクチンというタンパク質が関与する。
光合成は光化学反応とカルビン回路の2つの段階に大別される。光化学反応は光エネルギーからNADPHとATPを合成する過程で、カルビン回路はNADPHとATPを使ってCO2を固定・還元して炭素数3の化合物(グリセルアルデヒド3-リン酸)を合成する過程である。光化学反応が行われるのはチラコイド膜である[6]。カルビン回路はストロマで行われる[6]。カルビン回路の産物として得られたグリセルアルデヒド3-リン酸は,葉緑体内ででんぷんに変換され蓄積する。このように光エネルギーを使って水を酸化し、二酸化炭素を還元して、でんぷんを生成する反応が葉緑体の中で完結する。
葉緑体を持たない光合成原核生物では細胞膜か細胞膜が何層も陥入してできたクロマトホアで光化学反応が行われる[7]。
緑色植物の光合成
現在、最も研究の進んでいる酸素発生型光合成は緑色植物の光合成経路である。緑色植物の光合成経路は基本的に全ての酸素発生型光合成に応用可能であり、上記に上げられる生物群全てに以下の経路を当てはめても良い。酸素発生型光合成経路の最大の特徴は「水分子を電子供与体として用いることができる」という点である。水は酸化還元電位の高い酸素原子とそれの低い水素原子の結合した安定な物質である。この「水の光分解」を開発したことが、現在の酸素呼吸型生物の発展を生んだともいえる。
チラコイド膜では、クロロフィル(光合成色素)が光エネルギーを使って水を分解、プロトン(H+)と酸素分子(O2)、そして電子(e-)を作る。このときにできた電子によってNADP+(酸化型)からNADPH(還元型)が作られる。さらに、チラコイド膜内外のプロトン濃度勾配を利用して、ATP合成酵素によってアデノシン三リン酸 (ATP) が作られる。以上が光化学反応(明反応)である。
次にチラコイド膜の外側にあるストロマ(葉緑体基質)で、光化学反応で作られたNADPHとATPを使って二酸化炭素を固定・還元して糖が作られる。この一連の反応は酵素反応(暗反応)である。
光化学反応
光化学反応とは光エネルギーを化学エネルギーに変換する系である。光を必要とするため明反応とも呼ばれる。狭義には光エネルギーが関与する光化学系II(PSII)および光化学系Iの反応を指すが、広義には光化学反応に関わる電子伝達系のすべての反応を指す。
光化学反応は、光化学系II(PSII)、シトクロムb6f、光化学系I(PSI)の3種のタンパク質複合体で構成され、これらはすべてチラコイド膜に存在する。PSIIとシトクロムb6f の間はプラストキノン(PQ)、シトクロムb6f とPSIとの間はプラストシアニン(PC)で結ばれている。PSIIに光(hν)が当たることによってH2OからNADP+に電子が流れ(青矢印)、プロトンがチラコイドルーメンに取り込まれる(赤矢印)。また、酸素発生複合体(OEC)によって水が分解されて酸素が発生するときもプロトンがチラコイドルーメンに生成する。チラコイドルーメンとストロマの間にできたプロトンの濃度勾配の浸透圧エネルギーによってATP合成酵素がATPを合成する。ATP合成酵素は1秒間に17回転し、ADPからATPを合成しているのである。
光化学反応の収支式は以下の通りである。
- <ce>12H2O\ + 12NADP^+ -> 6O2\ + 12 NADPH\ + 12H^+(in)</ce>
- <ce>72H^+(in)\ + 24ADP\ + 24Pi -> 72H^+(out)\ + 24ATP</ce>
生じた、NADPHおよびATPはストロマにて行なわれるカルビン回路で使用される。また生じるATP数は理論的なものであり、実際にはプロトンの漏れがチラコイド膜外に発生していると見られ、24ATPを生じているとは考えにくい。事実、カルビン回路に使用されるATP数は光化学反応で生じるATP数よりも少ない。
Z機構
植物では光化学反応は葉緑体のチラコイド膜で起こり、光エネルギーを使ってATPとNADPHを合成する。狭議の光化学反応は、非循環的電子伝達系と循環的電子伝達系の2つの過程に分けられる。非循環的電子伝達系ではプロトンは光化学系II内のアンテナ複合体に光が捕獲されることによって獲得される。光化学系IIの光化学系反応中心(RC)にあるクロロフィル分子がアンテナ色素から十分な励起エネルギーを得たとき、電子は電子受容体分子(フェオフィチン)に運ばれる。この電子の動きを光誘起電荷分離と呼ぶ。この電子は電子伝達系を移動するが、これをエネルギー勾配で表したのがZ機構(Z-scheme)である[8]。ATP合成酵素はエネルギー勾配を使って光リン酸化によってATPを合成するが、NADPHはZ機構の酸化還元反応によって合成される。電子が光化学系Iに入ると再び光によって励起される。そして再びエネルギーを落としながら電子受容体に伝えられる。電子受容体によって作られたエネルギーはチラコイドルーメンにプロトンを輸送するのに使われている。電子はカルビン回路で使われるNADPを還元するのに使われる。循環的電子伝達系は非循環的電子伝達系に類似しているが、これはATPの生成のみを行いNADPを還元しないという点が違う。電子は光化学系Iで光励起され電子受容体に移されると再び光化学系Iに戻ってくる。ゆえに循環的電子伝達系と呼ばれるのである。
カルビン回路
カルビン回路は暗反応とも呼ばれる過程で、二酸化炭素の固定・還元を行なう炭酸固定反応である。カルビン回路は複数の酵素と中間代謝物からなる複雑な回路であるが、リブロース1,5-ビスリン酸カルボキシラーゼ/オキシゲナーゼ(RubisCO)を初発酵素とし、炭素数5の化合物リブロース1,5-ビスリン酸と二酸化炭素から炭素数3の化合物3-ホスホグリセリン酸2分子を生成する二酸化炭素の固定反応から始まる。3-ホスホグリセリン酸は還元され、グリセルアルデヒド3-リン酸を生成する。二酸化炭素の固定反応を継続するためには、産物として生じたグリセルアルデヒド3-リン酸からRubisCOの基質となるリブロース1,5-ビスリン酸を再生産しなければならない。このため、5分子のグリセルアルデヒド3-リン酸(炭素数3の化合物)が3分子のリブロース1,5-ビスリン酸(炭素数5の化合物)へ転換される。
これら一連の「二酸化炭素の固定・還元・基質の再生産」の過程がカルビン回路を構成する。従ってカルビン回路が3回転することにより、3分子の二酸化炭素が固定され、1分子のグリセルアルデヒド3-リン酸を生成する。この過程で、光化学反応によって生じたNADPHおよびATPが消費される。収支式で示すと以下のようになる。
- <ce>CO2\ + 5H2O\ + 6NADPH\ + 9ATP -></ce>
- グリセルアルデヒド3-リン酸 <ce>+ 6NADP^+\ + 9ADP\ + 8Pi</ce>
光化学反応を含めて光合成の収支式をまとめると以下のようになる。
- <ce>6CO2\ + 12H2O -> (CH2O)6\ + 6H2O\ + 6O2</ce>
この式は好気呼吸の収支式の逆反応であり、炭素消費および固定の収支が極めて巨大な生態系視野でもうまく行くことが理解できる。
光合成の分類
光合成とは狭義には『緑色植物の行なう酸素発生型光合成』を指すが、広義には『光合成細菌の行なう酸素非発生型光合成』を含める。さらに広い定義では高度好塩古細菌の行うレチナールを使った光エネルギー変換(ロドプシン型光合成)を含めることもある。光合成を行なう生物群およびその光合成の種類について以下に記す。
酸素発生型光合成は全ての生物にわたって反応中心、電子伝達系などの相同性が高い。唯一集光色素のみがかなり異なっておりカロテノイドではβ-カロテン、クロロフィルではクロロフィルaのみが共通に存在している。酸素非発生型光合成は系統樹上極めて古く、光化学系を一つしか有していない。緑色硫黄細菌の光化学系は光化学系Iと相同性が高く、紅色細菌の光化学系は光化学系IIと相同性が高い。
各光合成の収支式は以下の通りである。なお、電子供与体および電子受容体を太字で示す。
- 一般式
- <ce>CO2\ + 2 H2D</ce>(電子供与体)<ce> -> (CH2O)_n </ce>(炭水化物)<ce> + H2O\ + 2 D </ce>(酸化を受けた電子供与体)
光合成速度と呼吸速度
光合成を行う植物や一部の動物(ミドリムシなど)は、同時に呼吸も行っている。したがって、光が当たっている状態で放出されるO2量は、見かけの光合成速度である。これに対し、真の光合成速度は見かけの光合成速度に呼吸速度を加えたものである。
光合成によるCO2吸収速度と呼吸によるCO2放出速度が同じになる光の強さを、補償点という[9]。この時、見かけの光合成速度は0になる。
光合成速度と外的要因
光合成速度は、光の強さはもちろんCO2濃度や温度などの外的要因を強く受ける。光合成速度は、これらの要因のうち、最も少ないものによって決定される。この、光合成速度を決定する要因を限定要因という[10]。
例えば10℃と30℃の環境下でその他の条件を同じにして光の照度を徐々に強めていったとき、10℃の時に速度の上昇が停止する照度と、30℃の時の照度では、30℃の時の照度が一般的に高い。つまり、10℃の時は温度が光合成速度の限定要因になっている。光をそれ以上強くしても光合成速度が増加しなくなる光の強さを、光飽和点という。もちろん、照度・温度・二酸化炭素濃度のどれもが限定要因になり得る。これらの関係は、長さの異なる板で箱を作ったとき、水は長さの最も短い板の高さまでしか入ることのできない事を例に説明される事が多い。
酸素非発生型光合成経路
酸素非発生型の光合成を行う生物は、主たる代謝として二酸化炭素を固定するかしないかによってその栄養的分類が異なる。それらの分類を以下に示す。
- 光合成独立栄養生物 - エネルギー源として光を利用し、炭素源として二酸化炭素を用いる(紅色硫黄細菌、緑色硫黄細菌)。
- 光合成従属栄養生物 - エネルギー源として光を利用し、炭素源として有機化合物を用いる(紅色非硫黄細菌、緑色非硫黄細菌)。
酸素非発生型光合成もそれぞれ、光化学反応、カルビン回路に該当する反応系が存在するが、そうした言葉を当てはめることはない。そのため、それぞれ光化学反応系および炭素固定経路と呼称される。光化学系複合体は通常1つしか持っておらず、電子は循環的に光化学系内を回転する(循環的光リン酸化)か、非循環的に酸素やNAD+に電子伝達される(非循環的光リン酸化)。また緑色硫黄細菌の光化学系は緑色植物の光化学系Iと相同性が高く、紅色細菌の光化学系は同じく光化学系IIと相同性が高い。
光合成独立栄養生物の場合は炭素固定経路にはカルビン回路を用いているケースが多いが、例外的に Chlorobium limicola f. thiosulfatophilum は還元的クエン酸回路を用いて炭酸固定を行う。光化学系では硫化水素などを酸化することで還元力を生んでいる。
光合成従属栄養生物の多くもカルビン回路による炭素固定を行って独立栄養的に生育できることが知られている。また、従属栄養的に生育する場合も有機物代謝系より生じた余剰還元力の調整のために炭素固定を行う。光化学系では循環的光リン酸化によるATPの合成が行われている。
光合成に関わる年表
- 18世紀
- 1772年 イギリスのジョセフ・プリーストリーは、ハッカとネズミの実験から「汚れた空気」は植物によって浄化されることを発見した。
- 1779年 オランダのヤン・インゲンホウスは水草の実験から、植物が「きれいな空気」を出すには「光」が必要であり、光がないときは逆に空気を汚染することを発見した。
- 19世紀
- 1804年 スイスのニコラス・テオドール・ド・ソシュールは、ソラマメの実験から、根から吸収されていると考えられていた二酸化炭素は葉から吸収されていたことを発見、さらに、二酸化炭素が存在しないと植物は生きられないことを発見した。
- 1862年 ドイツのユリウス・フォン・ザックスは、植物は日光に当たると二酸化炭素からデンプンを合成し、それで成長していることを発見した。
- 1893年 アメリカのチャールズ・バーネスは光合成(Photosynthesis)という言葉を作り、論文中でその定義を発表した。
- 20世紀
脚注
- ↑ 吉田茂男 (1997), 植物化学調節実験マニュアル, 全国農村教育協会, p. 50, ISBN 9784881370636
- ↑ 2.0 2.1 2.2 2.3 2.4 『ヴォート生化学 第3版』 DONALDO VOET・JUDITH G.VOET 田宮信雄他訳 東京化学同人 2005.2.28
- ↑ 3.0 3.1 3.2 『Newton 2008年4月号』 水谷仁 ニュートンプレス 2008.4.7
- ↑ 細辻豊二 (1986), 最新農薬生物検定法, 全国農村教育協会, p. 29, ISBN 9784881370247
- ↑ 小森栄治 (2006), 向山洋一, ed., 中学校の「理科」を徹底攻略, PHP研究所, p. 101, ISBN 9784569655666
- ↑ 6.0 6.1 Lack, A. J. (2002), 岩渕正樹 訳; 坂本 亘 訳, ed., 植物化学キーノート, シュプリンガー・ジャパン, pp. 156-162, ISBN 9784431709787
- ↑ Hames, B. David; Hooper, N. M., 田之倉 優 訳; 村松知成 訳; 阿久津秀雄 訳, ed., 生化学キーノート, シュプリンガー・ジャパン, p. 391, ISBN 9784431709190
- ↑ Mohr & Schopfer 1998, pp. 165-168
- ↑ Mohr & Schopfer 1998, pp. 222-226
- ↑ Mohr & Schopfer 1998, p. 225
参考文献
- Mohr, Hans; Schopfer, Peter (1998), 網野真一 訳; 駒嶺穆 訳, ed., 植物生理学, シュプリンガー・ジャパン, ISBN 9784431707899
関連項目
外部リンク
- 光合成の応用研究開発
- 光合成に関係する生体分子のSITE例(生活環境化学の部屋)
- Animation and Graphics / Photosynthesis and Cellular respiration)